Samuel Coleridges berühmtes Gedicht „Der Raureif von The Ancient Mariner‘ zitiert: ‘Wasser, Wasser, überall, kein Tropfen zum Trinken!’ Mit diesen berühmten Zeilen deutete Coleridge an, dass er kein Wasser zum Trinken hatte, obwohl er von einem Ozean umgeben war. Er erwähnte auch, dass er einen Albatros getötet habe (was laut lokaler Überlieferung allen auf dem Schiff Unglück bringt). Natürlich bekräftigt er mit seinen berühmten Zeilen auch das allgemein bekannte Wissen, dass 75 % der Erdoberfläche Wasser haben. Darüber hinaus wissen wir, dass der menschliche Körper zu 60 % aus Wasser besteht. Daher erweist sich Wasser (ein einfaches Molekül) als entscheidend für alle Prozesse.
Damit die Schüler mehr über dieses bekannte Phänomen (im Detail) erfahren, geben Chemielehrer an Hochschulen Hausaufgaben zu den chemischen Eigenschaften von H2O, seiner Struktur, Umweltbedeutung usw., um ihr tiefes Verständnis zu ermitteln. Studenten, die sich über die chemischen Eigenschaften, die Struktur und die Gesamtbedeutung im Klaren sind, haben jedoch häufig Schwierigkeiten, innerhalb der engen Frist gut recherchierte und einzigartige Arbeiten zusammenzustellen. Glücklicherweise gibt es mehrere namhafte Websites zum Nachhilfeunterricht (z. B TopHomeworkHelper) bieten 360-Grad-Chemie-Hausaufgabenhilfe zu grundlegenden und fortgeschrittenen Themen an.
Ihr maßgeschneiderter Nachhilfeunterricht ermöglicht es den Studierenden, ihr Fach-/Konzeptwissen zu erweitern, ihre akademischen Schreibfähigkeiten zu verbessern und einreichungswürdige Arbeiten für hervorragende Noten vorzubereiten. Sie können es ausprobieren, wenn Sie ähnliche Schwierigkeiten haben, bestimmte Chemiethemen im Lehrplan zu verstehen.
Im Folgenden erläutern wir jedoch alles rund um den Titel anschaulich, um Ihnen den Einstieg in Ihre Hausaufgaben zu erleichtern.
Die chemischen Eigenschaften von Wasser
Als chemischer Stoff reagiert (H2O) mit vielen Stoffen unter Bildung verschiedener chemischer Verbindungen.
Redox Reaktion: Als wunderbare Wasserstoffquelle (mit zwei Wasserstoffatomen, die sich kovalent an ein Sauerstoffatom binden) reduzieren die elektropositiven Elemente Wasserstoffmoleküle.
Während der Photosynthese wird H2O reduziert und zu O2 oxidiert, was für Redoxreaktionen von entscheidender Bedeutung ist. (Beispiel ansehen)
![]()
Von Natur aus stimmungsvoll: Viele wissen vielleicht, dass H2O als Base und Säure dienen kann. Das deutet darauf hin, dass es von Natur aus atmosphärisch ist. (Beispiel ansehen)
Saures Verhalten:
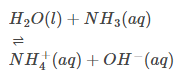
Grundverhalten:
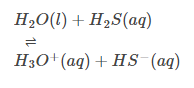 Hydrolysereaktion: Es weist vor allem aufgrund seiner Dielektrizitätskonstante auch eine starke feuchtigkeitsspendende Tendenz auf und kann mehrere ikonische Verbindungen auflösen. Bestimmte ionische und kovalente Verbindungen können hydrolysiert werden.
Hydrolysereaktion: Es weist vor allem aufgrund seiner Dielektrizitätskonstante auch eine starke feuchtigkeitsspendende Tendenz auf und kann mehrere ikonische Verbindungen auflösen. Bestimmte ionische und kovalente Verbindungen können hydrolysiert werden.
Sicher Hausaufgabenhilfe an der Uni von TopHomeworkHelper.com und erhalten Sie kostenlosen Zugang zu zahlreichen Antwortlösungen/Schreibnotizen in der Chemie.
Mehr zu H2O-Eigenschaften
- Molmasse – 8,01528(33) g/mol
- Feststoffdichte – 0,9167 g/ml bei 0 °C
- Flüssigkeitsdichte – 0,961893 g/ml bei 95 °C, 0,9970474 g/ml bei 25 °C, 0,9998396 g/ml bei 0 °C
- Schmelzpunkt – 0 Grad C
- Siedepunkt – 100 °C
- Säure – 13,995
- Dampfdruck – 0,032176 atm/3,1690 Kilopascal
- Viskosität – 0,890 cP
- Wärmeleitfähigkeit –0,6065 W/m·K
- Brechungsindex – 1,3330 (nD)
- Basizität – 13,995 (pKb)
Die Chemie der Wasserstruktur
Die chemische Struktur von Wasser besteht aus zwei verschiedenen Wasserstoffatomen, die sich mit einem einzelnen Sauerstoffatom verbinden. Aufgrund der höheren Elektronegativität der Sauerstoffatome weist es polare kovalente Bindungen auf. Das Sauerstoffatom lockt im Gegensatz zu Wasserstoffatomen die gemeinsamen Elektronen der kovalenten Bindungen stärker an. Daher werden die Sauerstoffatome (teilweise) negativ geladen, während die Wasserstoffatome eine teilweise positive Ladung erhalten. Aufgrund der zwei freien Elektronenpaare am Sauerstoffatom nehmen die Atome dann eine gebogene Struktur an. Die gebogene Form des Wassermoleküls entsteht dadurch, dass sich polare O-H-Bindungen nicht gegenseitig aufheben und das gesamte Molekül polar ist.
Darüber hinaus ziehen sich die polaren Bindungen gegenseitig durch die Dipol-Dipol-Kräfte an (das positive Ende eines Moleküls wird vom negativen Ende des benachbarten Moleküls angezogen). In Wasser haben die polaren O-H-Bindungen in der Nähe der Wasserstoffatome eine geringe Elektronendichte, wobei jedes H2-Atom von den einzelnen Elektronen eines benachbarten O-Atoms angezogen wird. Sie werden als Wasserstoffbrückenbindungen bezeichnet und sind stärker als alle normalen Dipol-Dipol-Kräfte.
Umweltbedeutung
Da die Weltbevölkerung jedes Jahr boomt, Auch die Umweltbedeutung und der Bedarf an nutzbarem Wasser nehmen zu.
Wasser ist auch wichtig für die Ernährung, das Wachstum und die Pflege verschiedener Pflanzen und Tiere (sogar für die Bewegung und Zucht von Fischen). Regelmäßige Bewässerungen für Blütenpflanzen bieten auch Insekten, Reptilien, Fröschen und Säugetieren Nahrung und Schutz. Sogar Waldvögel reagieren gut auf gesunde Feuchtgebiete. Sie können sich leicht ernähren und ausziehen, um Pflanzen zu bestäuben und Insekten und Schädlinge zu regulieren.
Die Öffentlichkeit muss den Wert des Wassers stärker anerkennen. Sauberes Wasser ist für die Landwirtschaft, die Viehhaltung, die Abwasserentsorgung und die Erhaltung des umgebenden Ökosystems von entscheidender Bedeutung. Wasser trägt zur Wiederherstellung und Aufrechterhaltung des natürlichen Flusses in Flüssen, Feuchtgebieten, Bächen usw. bei und unterstützt die Lebensräume in Überschwemmungsgebieten.
Daher ist es für die Weltregierung und andere offizielle Stellen wichtig, zum Wohle aller ein gesundes, erneuerbares und widerstandsfähiges Wassersystem aufrechtzuerhalten.
Source: Die Chemie des Wassers: Eigenschaften, Struktur und Umweltbedeutung






